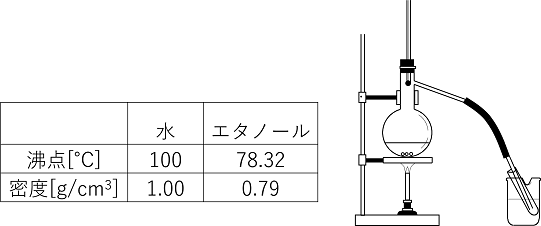
に状態変化し,そのときの温度を沸点とよび,沸点は物質 によって決められていることを学習する。 ここでは,この性質を利用した蒸留の実験を行う。身近 な物質である水(沸点 ℃)とエタノール(沸点 ℃) が混合した液から,エタノールを取り出す。水-アルコール混合系はいくつかの熱力学異常を示 す。最も顕著なのは超音波音速vUS の組成依存性で、 あるアルコール濃度(エタノールで約15モル%、メタ ノールではやや温度依存して1030モル%付近)で極 大を示す(図1(a)参照)。密度の組成依存性が例えば 水 ( 沸点 100 °C )と エタノール (沸点7 °C )の混合物が沸騰する際、エタノールの濃度が低ければ気相におけるエタノール濃度は液相のそれより高い。
Web教材イラスト図版工房 理 10 広島 問 01 02
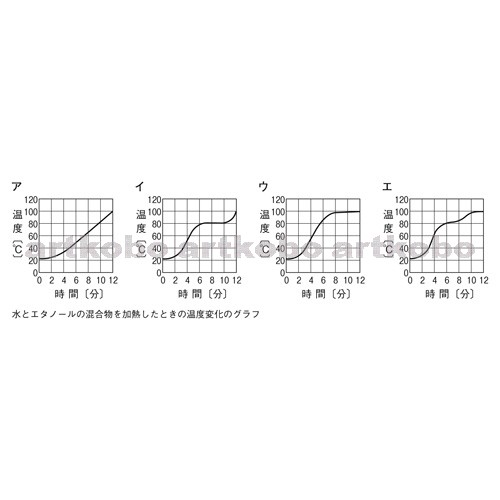
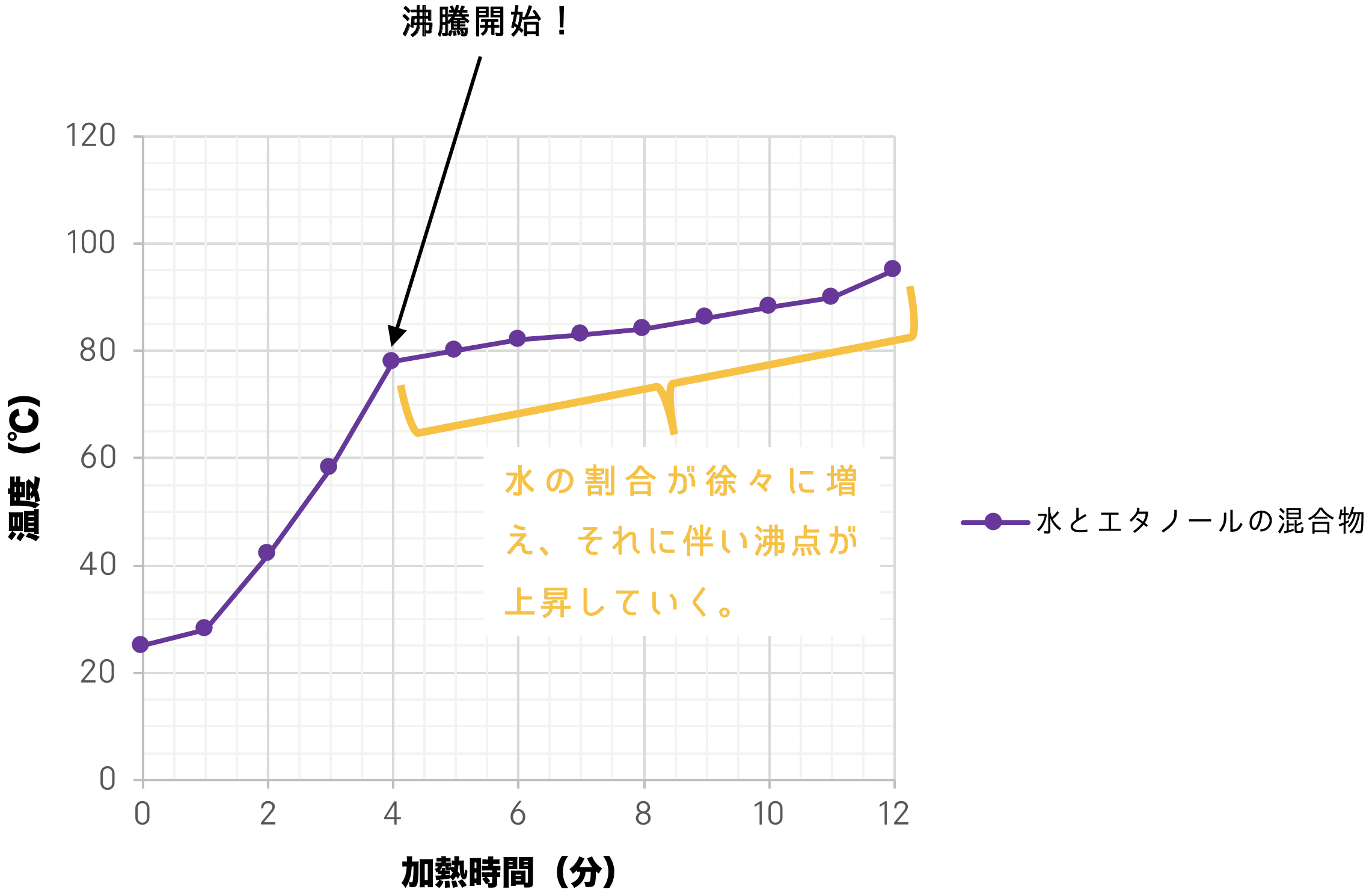
水とエタノールの混合物の温度上昇
水とエタノールの混合物の温度上昇-0wt% 10wt% wt% 30wt% 40wt% 50wt% 60wt% 70wt% 80wt% 90wt% 100wt% 65 092 058水エタノール共沸混合物の沸点は7 °c で、水およびエタノール単体の沸点より低い。 このような共沸混合物の沸点を 極小共沸点 という。 一方、水と 塩化水素 (沸点 −80 °C )の混合物は塩化水素%の濃度で共沸混合物となり、その沸点は109 °C である




状態変化 蒸留の実験の問題 無料で使える中学学習プリント
4 4 第6 章 演習問題解 解答 N 2 は,076 g / 280 g mol−1= 0027 mol,O 2 は,024 g / 3 g mol −1= mol この混合気体におけるN 2 とO 2 のモル分率をx N2, x O2 とすると x N 2 = 0027 =07 x O 2 = =0217 p total = 052 atm より p N2 = 07 ´ 052 = 0407 atm p O2 = 0217 ´ 052 = 0113 atm 問10 トルエン(t)と水に塩分などの不純物が溶け込むと、沸点は上がる。ただし、水1kgに溶質を1mol溶 かした水溶液では、沸点は約05℃しか上昇しないので、水道水程度の不純物では、この 上昇は全く無視してよい。 (3) 測定方法によるもの 小学校でよく使う棒状温度計は反応温度を保つには,それなりの条件が必要なのである。 1 ジエチルエーテルの生成 反応液(エタノールと濃硫酸の混合物)の温度を130~140℃または160~170℃に保つのは加熱の強さではなくエタノールと濃硫酸の割合である。
Gの水を ℃上げるために必要な熱量は × だから 400 × 50 = 000 000カロリーの熱が必要である。 答 000カロリー 水を混ぜる問題1 同じ温度の水を混ぜても温度は変わらない。 ℃の水400gと、℃の水500gを混ぜると、℃の水900gになる。埼玉県さいたま市岩槻区加倉3910 営業時間 ランチ 1100~1500 ディナー 1700~ 定休日 毎週木曜日 ※ご予約はお電話にて承ります。アは、「温度の変化の様子はまったく同じになる」というところが誤りです。 水を多くすれば100℃近くまで急に上がりますし、エタノールを多くすれば80℃あたりで温度上昇は止まるから です。 イ 混合割合によって、温度の変化の様子は違ういます。
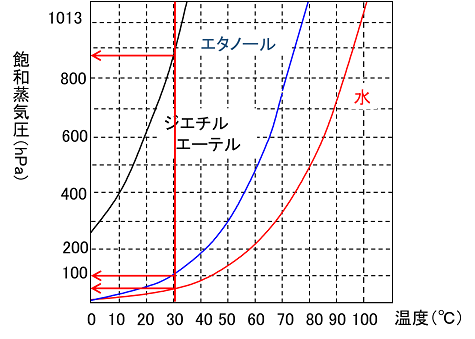
図3と同じく x = 030 、 y = 073 に対してその平衡温度は、 112 ℃ であることを示している。 図4 気液平衡線(沸点曲線、露点曲線) なお図4は、液相領域、気液混合領域、気相領域をも示している。水とエタノールの混合物を加熱 温度による物質の変化のようすを調べるために、エタノールを用いて実験を行った。次の問いに答えよ。 実験1 図1のように、ポリエチレンのふくろに液体のエタノールを少量入れて密閉し、熱い湯をかけたところ、図2の化学連載 第47回:蒸気圧降下と沸点上昇 液体を加熱していくと、液体内部に小さな気泡が生じ始めます。 この気泡は、液体が蒸発してできた蒸気の塊で、内部はその温度の飽和蒸気圧になっています。 さらに加熱を続けると、この小さな気泡は大きく
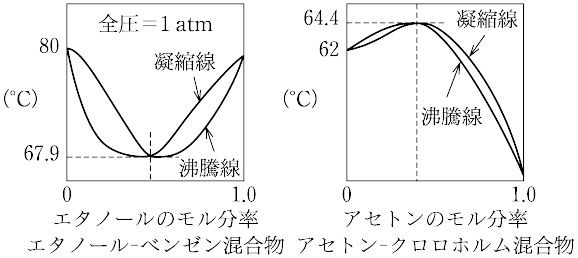



共沸混合物とは コトバンク
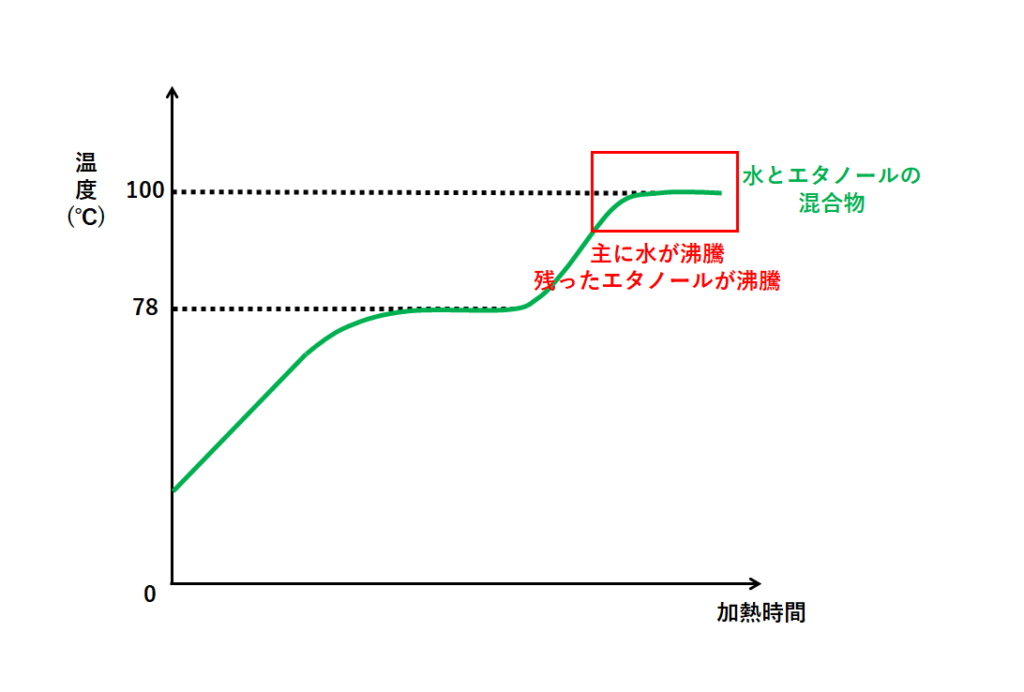



中1化学 蒸留 中学理科 ポイントまとめと整理
水エタノール共沸混合物(a成分が h2o、b成分がエタノール)はpii194に記載しており、共沸温度は℃、水の質量分率は0040とあります。 (2)『標準化学用語辞典』(第2版 丸善 053親水基と疎水基 エタノールc 2 h 5 ohやグルコース(ブドウ糖)c 6 h 12 o 6 などは水に良く溶ける。 このエタノールの分子は、分子中にヒドロキシル基 oh を持つ。エタノールでは、このヒドロキシル基の部分が、水分子と水素結合を生じて、エタノール分子が水和をする。比誘電率の温度依存性 十分低い周波数において、水の比誘電率の温度依存性は、以下の式で表される(出典:理科年表)。 \begin{align} \varepsilon_{\text{r}}(t)= t0131 \times 10^{2} t^{2}0046 \times 10^{4} t^{3} \label{eqdiele} \end{align} 図1 にその温度依存性を示し
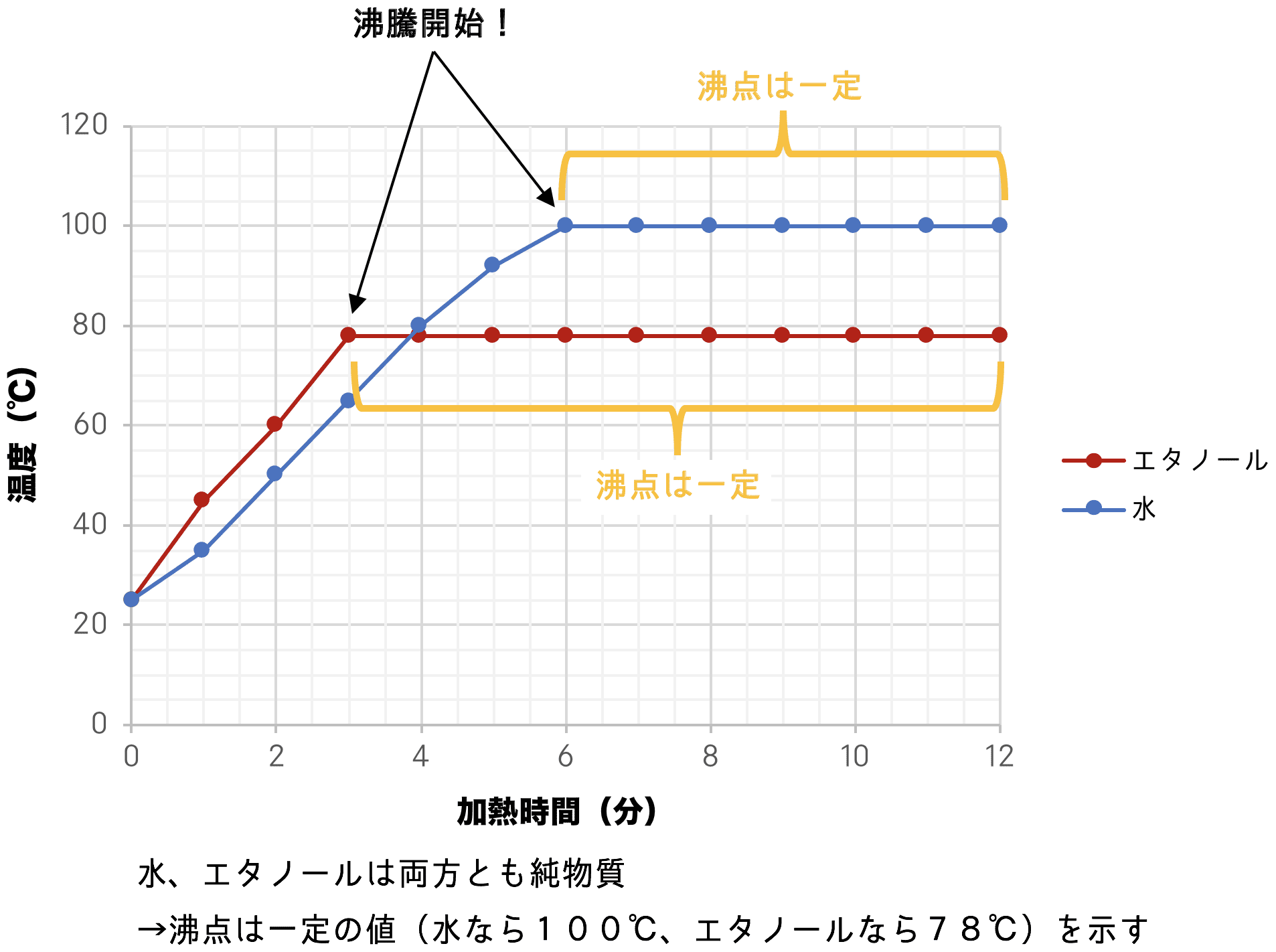



純物質と混合物 定義 違い 見分け方 例など 化学のグルメ
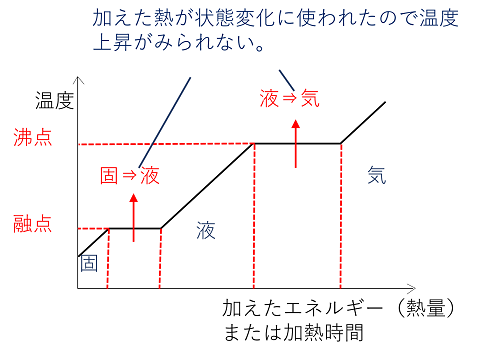



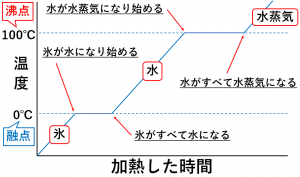
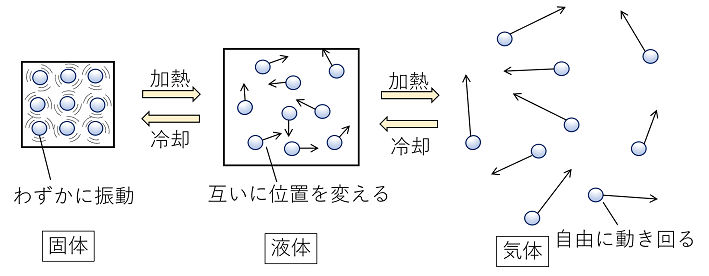
物質の三態と状態変化
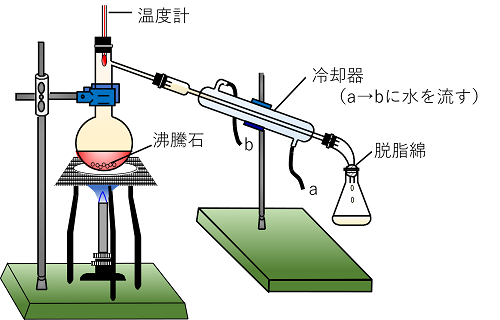
69vol% (55wt%) 10vol% (81wt%) 124vol% (10wt%) vol% (163wt%) 245vol% (wt%) 30vol% (247wt%) 362vol% (30wt%) 40vol% (334wt%)また、温度変化の仕方も混合する割合によって変わる。 例 水とエタノールの混合物を加熱した場合 水の沸点 エタノール の沸点 実験エタノールと水の混合物の加熱 図のような装置で、水とエタノールの混合物を加熱する。 温度計の球部は枝の高さに トップ > 化学 II > 第 1 部 物質の構造>第 4 章 溶液の性質> 第 1 節 溶解と溶解度 第 1 節 溶解と溶解度 溶解の機構 イオン結晶の溶解 塩化ナトリウムは水によく溶けるが,ベンゼンには溶けない。 塩化ナトリウムの結晶中では, Na + と Cl - が静電気力で強く結ばれている。
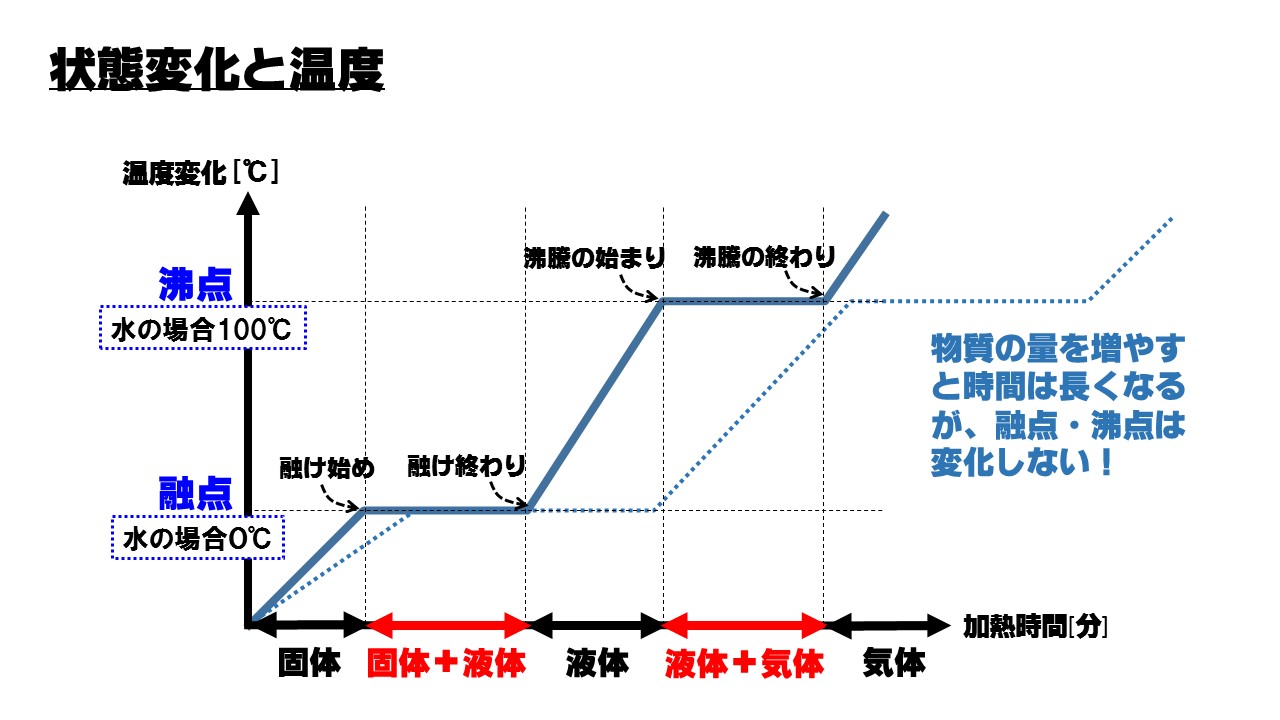



中1理科 物質の状態変化のポイントまとめ Atstudier
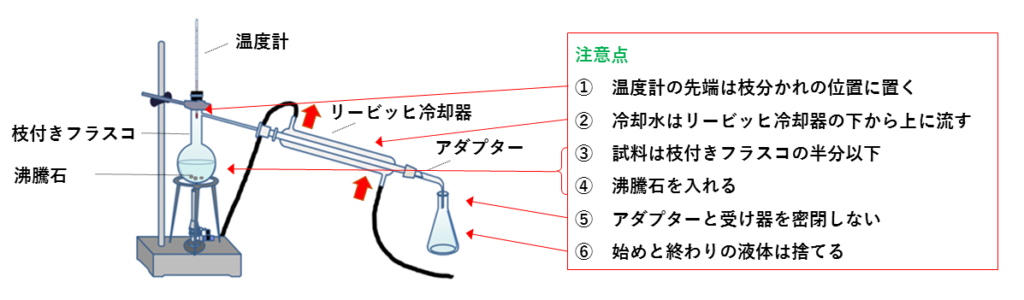



3分でわかる 蒸留と分留の意味と違いと覚え方を図と動画で徹底解説 サイエンスストック 高校化学をアニメーションで理解する
水の密度は温度が3984℃の時に最大となり、 g/cm 3 である。「水の不思議について」は別の記事がある。 液体の密度は特に指定がない場合には、この最大の密度となる温度の水を基準にすることになっている。エタノールに 濃硫酸 を混ぜて、130〜140℃に加熱すると分子間脱水が起こり、 ジエチルエーテル が生成する。 また、濃硫酸を混ぜた状態で160 170℃に加熱するか、活性アルミナ触媒の存在下で強熱する と、分子内脱水が起こり、 エチレン が生成する。液体の蒸気圧は温度の上昇とともに指数関数的に大きくなる。 る。実際に比較的似通った性質を持つ液体混合物について、αを一定とした理想溶液近似を適 (蒸気の組成)は液相の組成と関係なく一定になる。水蒸気蒸留はこのことを利用した手法




混合物の状態変化グラフと 理解を試す総合問題集 Menon Network




状態変化 蒸留の実験の問題 無料で使える中学学習プリント
二成分系混合液の蒸留 (精留) 目 的 なって塔内を下降する。塔内で上昇する蒸気と下降する液体とが 互いに接触、つまり向流接触 ③ 冷却水の元栓を開き、水の流れを確認したならば、操作盤の電源スイッチ をon にする。 この温度は 1 気圧の水塩化水素系の沸点の極大値であり、純水の沸点よりも高い。他の共沸化合物の例としては水とエタノールの混合物がよく知られている。1 気圧の水エタノール系では、エタノールの質量パーセント濃度が 960 wt% のとき沸点が極小と通常の溶質の場合、液体中の拡散係数はおよそ109 m 2 s1 程度の値をとります。 さきに評価したように、分子の平均速度を 100 m/sとし約 001 nm程度進んではでたらめに向きを変えると考えると、ちょうどこの程度の拡散係数がえられます。



理科の授業 水とエタノールの混合物の蒸留



状態変化と温度 固体 液体 気体 の達人
水と砂糖水とでは,水だけの方が早く蒸発するのを知っていますか。また,海水でぬれた水着は,真水でぬれた水着より乾きにくいですね。どうしてでしょう。 この章の学習内容は,次の通りです。 (1)蒸気圧降下 (2)沸点上昇 (3)凝固点降下実験16:エタノールの沸点 12 9 26(水)、28(金) 理科室 16年追記あり はじめに 本時はエタノールの沸点、次時『パラフィンを加熱、冷却する』を挟み、次々時にパルミチン酸の融点と凝固点を測定します。いずれも同じような実験装置で、同じような52 混合物 521 部分モル体積 大量の水に、1 mol の水を加えると、体積は18 cm3 増加 (25 °C) 大量のエタノールに、1 mol の水を加えると、体積は14 cm3 増加 (25 °C) 混合物中の成分i の部分モル体積 i p T nj i i n V V ≠ ⎟⎟ ⎠ ⎞ ⎜⎜ ⎝ ⎛ ∂ ∂ =,, (58)
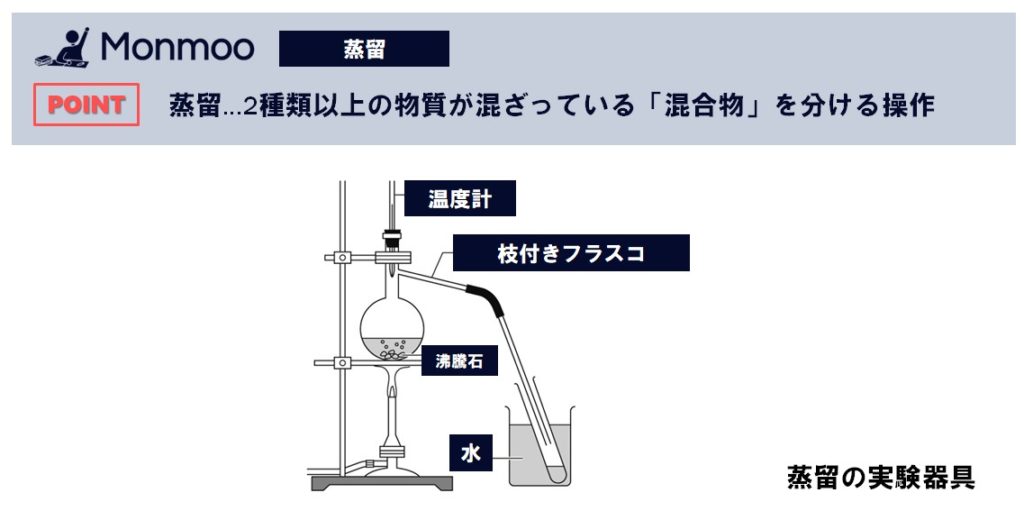



中1理科 蒸留 水とエタノールの混合物の実験 のポイント Atstudier




中1理科 混合物の状態変化と温度 練習編 映像授業のtry It トライイット
3 メスシリンダーで,エタノールを4mL と水5mL をはかりとる。そのとき,それぞれの液温を測定しておく。エタノールを水の入ったメスシリンダーに入れてよく混ぜる。温度変化と混合後の体積変化エタノールと水は共沸混合物となるので、蒸留による完全な分離は困難である。 今回は後で用いる反応において水の存在は問題にならないので、45%水エタノールの共沸混合沸点78℃で留出物を集める。 操作 エタノール100mLを常圧蒸留する。 蒸留の原理92 第12 章 水の相転移4 ~凝固点降下・過冷却~ 122 過冷却 1221 過冷却液体 熱平衡状態を保って水を冷却すると,水の温度は図124(a) のように時間変化する.平 らな部分が凝固点であり,0 ℃の水が潜熱を放出してエントロピーを減少させ,氷に相転 移している状態である.熱平衡状態は水から




混合物の状態変化グラフと 理解を試す総合問題集 Menon Network



1
水にまつわるエトセトラ 図1.エタノール水溶液の粘度のエタノールモル分率依存性。モル分率02程度のところで粘度が最大になることがわかる。 図3.大阪大学構内の竹薮から採取したクマムシの一種。乾燥した竹の落ち葉を水に浸し、沈殿物の中に



Http Koara Lib Keio Ac Jp Xoonips Modules Xoonips Download Php File Id 333



物質の三態と状態変化




働きアリ 覚え方




混合物の状態変化グラフと 理解を試す総合問題集 Menon Network



Http Www Fdtext Com Dan Fdn 1k2 Jyoutai Pdf



Http Www Iwakura Ed Jp Nihongo Rika c1 9 3 Pdf




理科 中1 32 状態変化するときの温度 水とエタノール編 Youtube



Http Koara Lib Keio Ac Jp Xoonips Modules Xoonips Download Php File Id 333




中1理科 物質のすがた テスト対策問題 Examee




Web教材イラスト図版工房 理 10 広島 問 01 02




スタディピア 物質の状態変化



Www Kyoiku Kensyu Metro Tokyo Jp 09seika Reports Files Kenkyuin Chu Rika 301 Chu Rika Pdf



蒸留




沸点 Wikipedia




Web教材イラスト図版工房 R C1 物質の状態変化 21



Http Honda Sci Yokohama Cu Ac Jp E7 90 86 E5 Ad A6 E9 A8 E7 94 A8 E6 Ba B6 E6 B6 B2 E5 8c 96 E5 Ad A6 3t Pdf



状態変化 印刷用まとめ




混合物の状態変化グラフと 理解を試す総合問題集 Menon Network



Http Www Iwakura Ed Jp Nihongo Rika c1 9 3 Pdf



Http Honda Sci Yokohama Cu Ac Jp E7 90 86 E5 Ad A6 E9 A8 E7 94 A8 E6 Ba B6 E6 B6 B2 E5 8c 96 E5 Ad A6 3t Pdf




状態変化 Flashcards Quizlet




中学校理科 第1分野 物質のすがた Wikibooks



状態変化 印刷用まとめ



Http Www Ginga Ac Jp Wpcms Wp Content Uploads 04 D53b91c5ffed64bff74f9 Pdf




混合物の状態変化グラフと 理解を試す総合問題集 Menon Network




中1理科 水とエタノールの温度変化 映像授業のtry It トライイット




中1化学 蒸留 中学理科 ポイントまとめと整理




Web教材イラスト図版工房 R C1m 水とエタノールの混合物の温度変化のグラフ 2



Miyaichi Myswan Ed Jp Wysiwyg File Download 1 1566



状態変化と温度 固体 液体 気体 の達人



蒸留




中1理科 混合物の状態変化と温度 練習編 映像授業のtry It トライイット




中1理科 物質のすがた テスト対策問題 Examee




混合物の状態変化グラフと 理解を試す総合問題集 Menon Network



物質の三態と状態変化



3




中1理科 エタノールの温度変化 映像授業のtry It トライイット



水とエタノールの混合物を分離する方法って何ですか 急ぎでお願いしま Yahoo 知恵袋



実験 水とエタノールの混合物の加熱




高校化学基礎 物質の沸点 映像授業のtry It トライイット



中1理科 状態変化 状態変化と温度 蒸留について理解しよう たけのこ塾 勉強が苦手な中学生のやる気をのばす




2枚目の蒸気圧曲線は 1枚目の物質の状態図の右上の部分を切り取ったグラフだと思ってい Clear




混合物の状態変化グラフと 理解を試す総合問題集 Menon Network




状態変化 蒸留の実験の問題 無料で使える中学学習プリント



水とエタノールの混合物を分離する方法って何ですか 急ぎでお願いしま Yahoo 知恵袋



純物質と混合物 定義 違い 見分け方 例など 化学のグルメ



Http Www Iwakura Ed Jp Nihongo Rika c1 9 3 Pdf




これは水とエタノールの混合物を加熱した後の温度変化を表したものです Clear




混合物の状態変化グラフと 理解を試す総合問題集 Menon Network



物質の三態と状態変化




中1理科 蒸留 水とエタノールの混合物の実験 のポイント Atstudier



1



なぜエタノールより水の方が早く沸騰するのに水とエタノールの混 Yahoo 知恵袋



物質の三態と状態変化



Http Honda Sci Yokohama Cu Ac Jp E7 90 86 E5 Ad A6 E9 A8 E7 94 A8 E6 Ba B6 E6 B6 B2 E5 8c 96 E5 Ad A6 3t Pdf




混合物の状態変化グラフと 理解を試す総合問題集 Menon Network




混合物の状態変化グラフと 理解を試す総合問題集 Menon Network
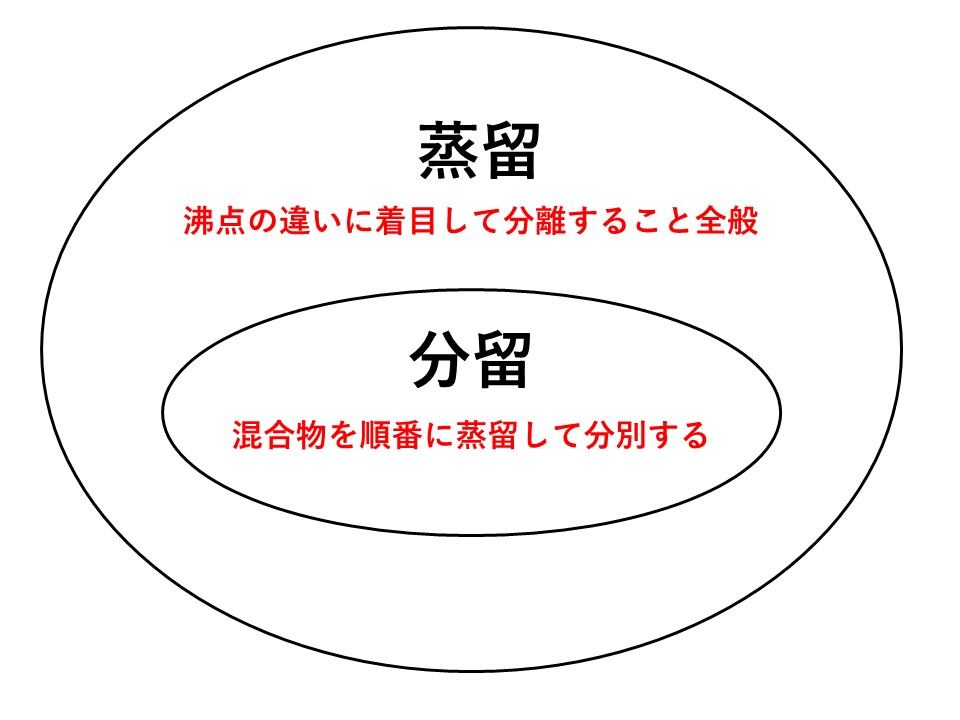



3分でわかる 蒸留と分留の意味と違いと覚え方を図と動画で徹底解説 サイエンスストック 高校化学をアニメーションで理解する
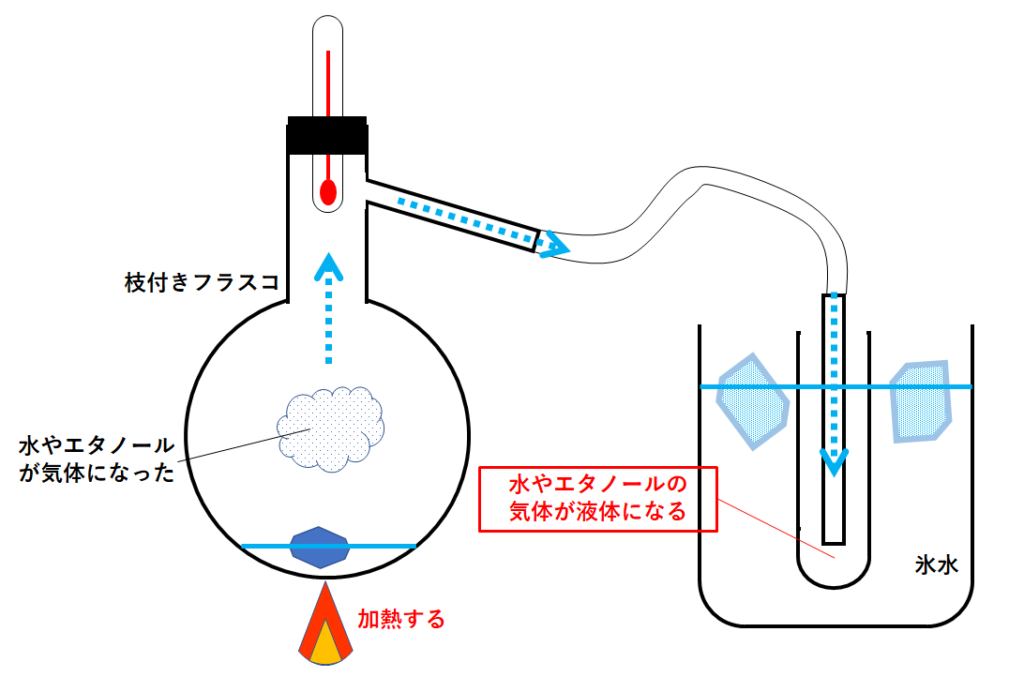



中1化学 蒸留 中学理科 ポイントまとめと整理



理科1年 化学




中1理科 混合物の状態変化と温度 練習編 映像授業のtry It トライイット



混合物を加熱したときのグラフは 他のとどのような違いがありま Yahoo 知恵袋



Http Www Iwakura Ed Jp Nihongo Rika c1 9 3 Pdf
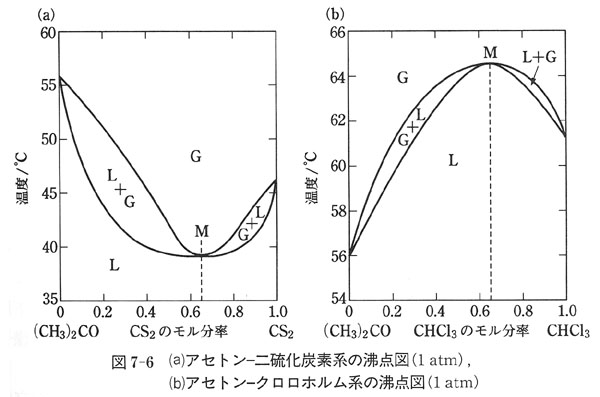



2 気相 液相平衡




中1 理科 化学 混合物の状態変化と温度 15分 Youtube




1 1混合物と分離 Chemistry




氷 水 水蒸気 変身しても 物質は 水 です うさはち物理教室




の問題の答えははなぜウの8分後なのですか なぜエだとダメなのでしょうか Clear




混合物の状態変化グラフと 理解を試す総合問題集 Menon Network




中1化学 蒸留 中学理科 ポイントまとめと整理




混合物の状態変化グラフと 理解を試す総合問題集 Menon Network




沸点 Wikipedia




中1化学 蒸留 中学理科 ポイントまとめと整理



Http Www Iwakura Ed Jp Nihongo Rika c1 9 3 Pdf




新編改訂化学基礎 ダイジェスト版




状態変化 蒸留の実験の問題 無料で使える中学学習プリント



理科1年 化学 物質の性質 気体 水溶液 状態変化 物質の性質 要点 金属 物体 ものを 外見から判断する場合 物質 ものを つくっている材料から判断する場合 金属の性質 みがくと光る 金属光沢 たたくとよくのびる 電気や熱を通す 非金属




水とエタノールの混合物を加熱したグラフに関しての問題について質問があります この大問 Clear



蒸留 原理 エタノールと水は共沸混合物となるので 蒸留による完全な分離は困難である 今回は後で用いる反応において水の存在は問題にならないので 4 5 水 エタノールの共沸混合沸点78 で留出物を集める 操作 エタノール100mlを常圧




混合物の状態変化グラフと 理解を試す総合問題集 Menon Network
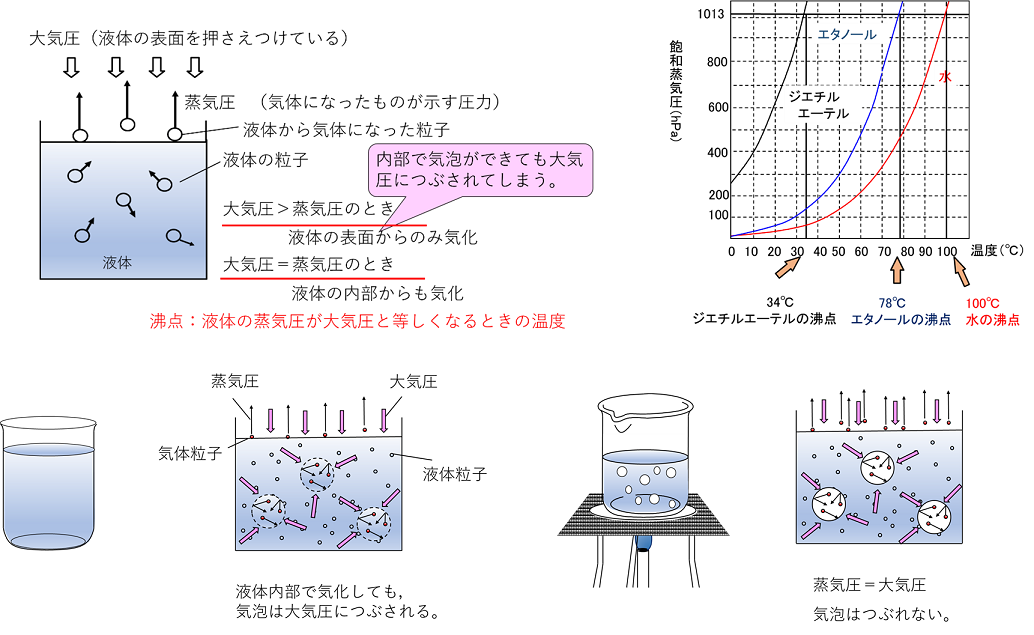



物質の三態と状態変化



3



Miyaichi Myswan Ed Jp Wysiwyg File Download 1 1566



この写真の問題で混合物が沸騰し始めたのは何分後ですか ア 2 Yahoo 知恵袋




混合物の状態変化グラフと 理解を試す総合問題集 Menon Network
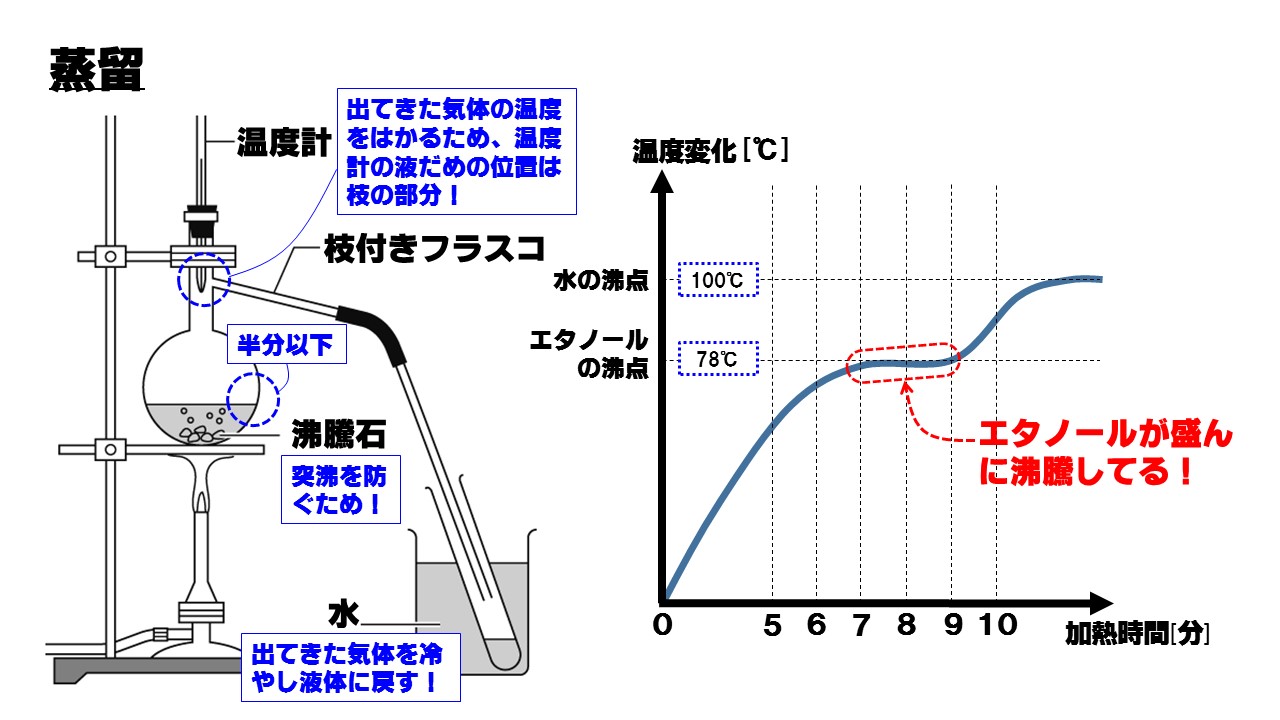



中1理科 蒸留のポイント Examee




中1理科 混合物の状態変化と温度 練習編 映像授業のtry It トライイット




沸点 Wikipedia
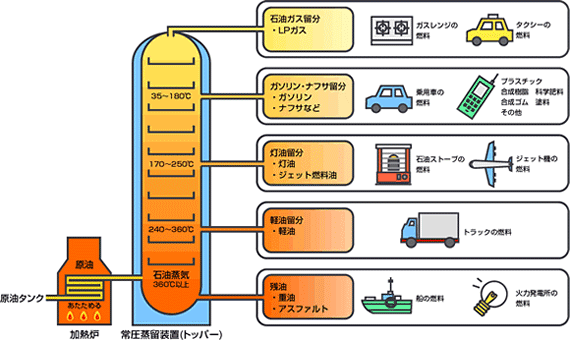



3分でわかる 蒸留と分留の意味と違いと覚え方を図と動画で徹底解説 サイエンスストック 高校化学をアニメーションで理解する



Http Www Iwakura Ed Jp Nihongo Rika c1 9 3 Pdf



0 件のコメント:
コメントを投稿